Oophorectomía en Histerectomía Después de los 40 años? Una Práctica que no Resistió el Proceso de Examinación
Como fue Publicado en el Volumen 5, Número 5 (Diciembre, 1996) de Menopause Management, (concerniendo el control (o manejo) de la Menopausia) , la publicación de la Sociedad de Menopausia en Norteamérica, para profesionales en el ámbito de la Salud Pública o Asistencia Médica.
Click here to watch the recent video interview of Dr. Cutler discussing her new book; Hormones and Your Health
*Please click here for more on pheromones and books from Athena Institute
By Winnifred B. Cutler (Athena Institute for Women's Wellness Research, Chester Springs, PA, USA)
Extirpación quirúrgica de gónadas (castración) altera el ámbito hormonal de varias formas diferentes que puede precipitar problemas de salud crónicas y un aumento en los costes. Más aún, regimenes diseñados unicamente con el fin de reemplazar el estrógeno pasan de alto las diversas contribuciones del ovario que impactan la vida de una mujer que este madurando.
- Introducción
- Cancer de Ovario- Riesgo
- Secuelas Post Oophorectomía
- Contribución de los Ovarios al Bienestar
- Alternativas a la Oophorectomía Prophyláctica
- Conclusión y Referencias
Introducción
Extirpación quirúrgica de gónadas (castración) altera el ámbito hormonal de varias formas diferentes que puede precipitar problemas de salud crónicas y un aumento en los costes. Más aún, regimenes diseñados unicamente con el fin de reemplazar el estrógeno pasan de alto las diversas contribuciones del ovario que impactan la vida de una mujer que este madurando.
Previamente, antes que los documentos de investigación empezaron a revelar los varios efectos negativos de este tipo de práctica, ovarios saludables eran removidos rutinariamente a través de histerectomías en Norteamérica en los años 70 y 80. Hoy en día, trabajos de investigación obtenibles a través de una simple investigación médica conducen a cuestionar seriamente la racionalidad y las normas éticas (en las mujeres que cuentan con más de 40 años de edad) concernientes a la práctica de remover rutinariamente ovarios saludables durante una histerectomía en el 99.9% de los casos con menos de un 1% de riesgo de cancer de ovario.
Aun así, médicos que lean la revista (Ginecológica de 1994 Oncología) Gynecologic Oncology1 verán esta frase: "Si el acceso a los órganos pélvicos es posible, mujeres que se someten a una intervención quirúrgica non ginecológica a los 40 o más deberían ser alentadas a considerar una oophorectomía prophyláctica." Aún así, en otro artículo discusiones adicionales cuestionan seriamente esta recomendación.2
Yo sugiero que la práctica de castración prophyláctica - la extirpación quirúrgica de ovarios saludables basado solamente en la posibilidad de enfermedades en el futuro - no resisten escrutiño. La posible devastación de ser afligido con un cancer de ovario tiene que ser balanceado cuidadosamente con la devastación existente en la extirpación de órganos saludables de estas mujeres que no corren alto riesgo de ser afligidas con el cancer de ovario.
Cancer de Ovario- Riesgo
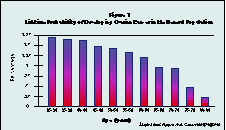
La existencia de cancer de ovario, o su prevención, [Imagen] parece ser la única razón racional para considerar una ovariectomía durante una histerectomía. El riesgo actual de cancer de ovario disminuye con la edad (vea la figura 1). La probabilidad de obtener cancer de ovario en la población general agrupado según edades depende altamente del historial familiar (vea la figura 2). Una mujer que no cuenta con una historia de cancer de ovario en la familia tiene aproximadamente un riesgo de 1% en su vida de contraer esta enfermedad.
Para hacer la pregunta, "¿La ovariectomía previene el cáncer de ovario?" para una paciente sin antecedentes familiares de cáncer de ovario es engañoso. La respuesta es "probablemente sí", pero el precio es demasiado alto para una mujer con un riesgo relativo de cáncer de ovario inferior al 1%. Después de revisar los factores de riesgo familiares y el papel de la ovariectomía profiláctica en la prevención del cáncer, Nguyen y colegas,5 a la vez que Herbst,6 concluyen que las intervenciones quirúrgicas puede que sean apropiadas solo para las mujeres diagnosticadas con el síndrome de cancer de ovario en el historial familiar. Esto es una enfermedad hereditaria autosomal que ocurre en menos de un 1% de todos los casos de cancer de ovario (Herbst, 1994), y produce un riesgo de un 50% de desarrollarse en un cancer de ovario durante la vida de una persona. Por contra, la presencia de uno, dos, o tres miembros de familia con cancer de ovario aumenta el riesgo en la vida de un 1% entre todas las mujeres, y hasta un 5% o 7% dependiendo del número de parientes afligidos (Nguyen, 94) (Vea Fig. 2).
Asumiendo un incidente anual de 22,000 casos de cancer de ovario en los Estados Unidos y combinando la información con el porcentage de estos cánceres que ocurren en mujeres entre la edad de 40 años o más los autores concluyen que 1000 mujeres pueden salvarse del cancer de ovario sometiendose a la castración rutinaria de todas las mujeres mayores de 40 años durante una histerectomía.
Continuando con esta lógica, Yo estimo que 399,000 castraciones innecesarias tendrían que ser practicadas durante una histerectomía para patologías benignas con el fín de prevenir 1000 casos de cancer ovárico en los EEUU por año. Ya que la práctica de histerectomía reduce un 30% a un 50% la probabilidad de desarrollar subsecuentes cánceres de ovario el riesgo en general de este tipo de cancer después de una histrectomía alcanza la mitad del riesgo de 1% en la vida de una persona. Ya que el riesgo de cancer de ovario también disminuye después de los 50 años, el riesgo de contraer un cancer de ovario en una mujer que no tiene ningún historial familiar alcance un tercio del porcentage. Por eso más de un 99.75% de las prácticas "ovariectomía prophyláctica" son innecesarias. El usar intervenciones quirúrgicas para salvar a 1000 mujeres con posible riesgo de contraer esta enfermedad, 400,000 mujeres tendrían que ser castradas.
Secuelas Post Oophorectomía
Desafortunadamente, el no obedecer con las prescripciones de HRT, a la vez que la identificación incorrecta de reemplazos hormonales terapéuticos adecuados produce serías secuelas después de oophorectomía prophyláctica. Si las mujeres no toman los regimenes hormonales prescritos, mostrarán tasas excesivas de enfermedades al corazón y osteoporosis mientras que solo reducirán moderadamente su muy bajo riesgo de contraer enfermedades poco comunes.
Alteraciones en la sexualidad son inevitables como resultado de las reducciones tanto de hormonas de estrógeno como de las hormonas androgénicas. Una lubricación vaginal adecuada requiere estrógeno y un líbido adecuado requiere suficiente circulación de andrógeno; deficiencias son inevitables si estas hormonas son reducidas.
Trabajos de investigación en primates subhumanos y subsecuentemente en humanos revelaron que endógenos opiates caen precipitadamente después de disrupciones quirúrgicas de los ciclos de estrógeno/progesterón.7 Ovariectomías pueden comprometer la atractividad sexual de una mujer en parte debido a la desaparición de sus secreciones axiliares pheromonales. En monos Rhesus, la castración elimina la producción de atrayentes sexuales (pheromones) y conduce a una pérdida inmediata de la capacidad de atraer al macho. Solamente cuando los esteroides sexuales son reemplazados apropiadamente o cuando las secreciones pheromonales son aplicados vaginalmente, solamente entonces el mono recobró la atención sexual del macho.8 Investigaciones de pheromones humanos se encuentra en una fase infantil y solo existen trabajos de investigación limitados que tratan con la pérdida del potencial del atractivo sexual que puede sufrir una mujer castrada.
Contribución de los Ovarios al Bienestar
Los estudios clásicos de ovarios humanos en una muestra representativa demuestra claramente un cambio inevitable de la infancia a la vejez. Después de haber alcanzado un tamaño máximo, el promedio de la masa del ovario disminuye en la mujer entre las edades 30-39. Pero aun así, la disminución es acompañada por un aumento en la cantidad concomitante del tejido stromal. El ovario postmenopáusico es rico en tejido stromal (que provee una fuente rica de andrógenos),9 a menudo alcanzando niveles más altos que durante los años fértiles. Mujeres sanas de mayor edad (60-98 anos de edad) demuestran una secreción activa hormonal: ellas alcanzan niveles de plasma de estradiol que alcanzan un promedio de 16 pg/ml; testosterona, 270 pg/ml; y DHEAS, 360 ng/ml. 10 (una disminución en DHEAS relacionada con la edad, cuenta con mucha documentación al respeto.11 y castración acelera la disminución por un 50%.12 Aún queda por ser clarificado si la disminución de DHEAS inducida por la castración refleja una dependencia adrenal por parte del ovario, algún aspecto a la contribución del ovario, o ambos. Aun así, ya que DHEAS es una hormona precursora a otros steroides sexuales, su rol es agrandado.
El potencial de beneficios a la salud que conyeva la circulación DHEAS ha alcanzado recientemente considerable atención en el ámbito científico, al igual que en los medios de comunicación. Su rol concerniente a la salud y al bienestar se hicieron aparentes a mediados de los años 90. Una investigación Medline de este tema revelará numerosos estudios publicados recientemente en DHEAS. La terapia de reenplazamiento DHEAS aún no ha sido adecuadamente estudiada pero el concepto empieza a difundirse dentro de la literatura. Solamente algunas breves nociones citadas más abajo demuestran el potencial que presenta la retención de ovarios al bienestar general (que apoya niveles naturales más altos de DHEAS):
Secreción de DHEA es mucho mas bajo en las mujeres con cancer de pecho y en varios estudios han demostrado niveles de plasma humanos subnormales de ambos DHEAS y DHEA en pacientes con cancer de pecho avanzado. DHEA inhibe tres procesos que contribuyen al desarrollo de tumores:
1) Activación metabólica de un carcinógeno a través de la activación de funciones oxidases mixtas
2) Promoveedor de estimulaciones de tumores a través de proliferaciones de la celula
3) Promoveedor de tumores de tipo- O2- formación.13
En 1994 Mason y sus colegas mostraron que la tasas de sobrevivimiento de cancer de pecho esta relacionado de forma significativa con niveles de plasma DHEA más elevados y con el status de tumores steroid receptores.14 Los niveles de DHEA por debajo del promedio del grupo fueron asociados con una disminución significativa en la sobrevivencia en mujeres. Fue particularmente aparente en tumores receptores positivos postmenopáusicos la asociación era más potente en los que eran nódulos axiliares negativos.14
Niveles de DHEAS altos en hombres fueron asociados con índices reducidos de enfermedades cardiovasculares mortales,15 a la vez que DHEA oral a mujeres postmenopáusicas aumento el riesgo de factores lípidos.16 Examinación de los archivos de 942 mujeres post-menopáusicas reveló que niveles más altos en la base de DHEAS son asociados con varios factores de riesgo enfermedades cardiovasculares 12 años más tarde: pero que este tipo de niveles no eran asociados con riesgos de mortalidad en estas mujeres17 Aunque dosis excesivas pueden ser peligrosas a la salud cardiovascular en mujeres, aparentemente estos resultados dispares suscitan el potencial del rol de DHEAS en la salud cardiovascular, un tema maduro para futuras investigaciones.
Castración corta a la mitad los niveles de DHEAS que ya están disminuyendo en mujeres que están envejeciendo
Las relaciones entre la absorción de calcio, serum DHEA y densidad mineral de las vértebras en mujeres post-menopáusicas ha sido investigado mucho antes en el año 1985. La mal absorción de calcio a sido un factor de riesgo significativo para la osteoperosis, y niveles de DHEA bajos y parece que representa un factor de riesgo independiente adicional.18 Más recientemente, el rol tanto de DHEA como de DHEAS ha sido sugerido en la regulación de funciones osteoblast humanas como fue mostrado en cultivos de celulas responsables de la síntesis y mineralización del hueso.19
DHEAS y DHEA affectan las celulas del cerebro de forma beneficial, aumentando los cultivos de celulas nerviosas en el cerebro del ratón.20 Pacientes que sufren de alzeheimer muestran que la disminución en DHEA relacionado con la edad, es casi 40% más bajo que otra gente de su edad y sin la enfermedad.21
El desarrollo y la proliferación de trabajos de investigación sobre el DHEA y el DHEAS es bastante extenso, lo suficiente como para permitir la evaluación dentro de los límites marcados por los conocimientos actuales. Inequivocadamente -castración corta a la mitad los niveles ya bajos de DHEAS en mujeres que están envejeciendo.12 Aunque hoy en día los efectos fisiológicos de DHEAS que no son reemplazados siguen sin saberse. Existe una base racional para la terapia de reemplazamiento de DHEA en mujeres postmenopáusicas. Estudios sobre la terapia de reemplazamiento de DHEA ya han empezado a aparecer, y eventualmente niveles óptimos y temas relacionados con la seguridad serán resueltas.22
Alternativas a la Oophorectomía Prophyláctica
En la presencia de masa ovárica, mejoramientos recientes en la metodología de detección de cancer ovárico ha disminuido la justificación para la extirpación de ovarios saludables. Técnicas que han sido mejoradas pueden aumentar profundamente el valor positivo pronosticado a un 97%.5,23,24 Según Weiner et al, 24 la imaginería del color del flujo transvaginal a través de un ultrasound doppler de pulsación puede detectar etapas aún en su fase inicial de cancer del ovario a causa del aumento dramático del flujo de sangre a la región en las etapas iniciales de cancer ovárico. Mientras que estos estudios solo recientemente han empezado a aparecer, puede que sean de algun beneficio en el futuro. Actualmente no existe ningún método de revisióon que ha demostrado ser útil en la reducción de la mortalidad cuando no existe ninguna masa. El rol del médico al informar al paciente debe ser el de:
1) Definir el problema (no existe ningún chequeo oficial)
2) Describir el verdadero riesgo, el cual es bajo, de contraer cancer de ovario
3) Aclarar los riesgos inminentes arraigadas en el metodo de la castración y sus efectos a la salud.
En cuanto a temores irracionales concernientes con el cancer los médicos deberían recomendar terapia o asesoramiento profesional, en lugar de castraciones innecesarias.
Mejores técnicas diagnósticas que existen hoy en día pueden salvar a la mujer de operaciones quirúrgicas innecesarias en casos donde exista presencia de masa ovárica.
Conclusión y Referencias
Conclusión
Mejores técnicas diagnósticas que pueden salvar a la mujer de operaciones quirúrgicas innecesarias dada la presencia de masa ovárica. Médicos deberían utilizar cursos de educación para aprender estos métodos de detecciones e incluirlos como el nuevo estandar de cuidado médico. El enfoque debería concentrarse en el desarrollo de mejores técnicas de detección en vez de convencer a las mujeres de aceptar una castración innecesaria para poder así prevenir un posible riesgo de contracción de cancer ovárico de menos de medio por cien.
Como consumidores de Salud Pública, las mujeres que están informadas tienen tendencia a ejercer sus derechos a tomar decisiones racionales. Las mujeres están aprendiendo sobre los efectos de la castración:
La reducción del bienestar, El tiempo, la energía y el dinero perdido.
El tiempo que tarda en recuperarse después de una operación quirúrgica pélvica antes de que puedan desempeñar actividades normalmente, y
El tiempo, la energía y el dinero perdido.
El aumento de la multitud de funciones asociados con los ovarios continua a ser expuesto a medida que avanzan los estudios de investigación. A medida que los consumidores de Salud Pública reconocen las contribuciones hormonales inclusive de ovarios que están envejeciendo, y las secuelas sexuales que ocurren después de su pérdida, es probable que digan "no". Más importante, a medida que las mujeres descubren lo bajo que es el riesgo a que contraigan cancer ovárico, para el 99.9% que no cuentan con el riesgo de tener un síndrome dominante autosomal, se espera que reaccionen vehementemente en contra de la sugerencia de castración.
A medida que el coste verdadero de "oophorectomía prophyláctica "es reconocido más extensamente entre los aseguradores en el ámbito médico y entre los consumidores más informados, la reducción de este tipo de práctica parece ser inevitable. Se espera que proveedores de recursos financieros nieguen fondos monetarios a operaciones quirúrgicas a medida que reconocen los costes tanto directos como subsequentes impuestos por operaciones quirúrgicas pélvicas.25
El potencial de un aumento en enfermedades cardiovasculares, osteoperosis, disfunciones sexuales, y sicopatología que viene como resultado de aumentos de oophorectomía prophylácticos todo ello aumenta los costes y la carga económica a la salud. Inevitablemente, se espera que organizaciones de salud administradas, al igual que la gente que paga por sí misma para servicios médicos, retengan los fondos monetarios para operaciones quirúrgicas "prophylácticas".?
Profesionales médicos informan sobre la proliferación de nuevos trabajos de investigación que van a dar la bienvenida a la reducción de operaciones quirúrgicas. El establecimiento médico está preparado para los cambios dramáticos en las estructuras financieras impuestas por el cuidado médico administrativo. El enfoque en mejores métodos de detección de las patologías y el entendimiento de la elegante sinfonía del cuerpo de una mujer que permanece intacto, aunque este envejeciendo, puede resultar en un mejoramiento en el cuidado médico.
Referencias
1) -Averette HE, Nguyen HN (1994) The role of prophylactic oophorectomy in cancer prevention. Gynecologic Oncology, 55: S38-S41
2) -Utian WH, GoldfarbJ. Ovarian management during radical hysterectomy in the premenopausal patient. Obstet Gynecol 1993;82(6):1042
3) -Hankinson SE, Hunter DJ, Colditz GA, Willett WC, Stampfer MJ, Rosner B, Hennekens CH, Speizer FE (1993) Tubal ligation, hysterectomy, and risk of ovarian cancer: A prospective study. JAMA, 270, 23: 2813-2818
4) -Prazzini F, Negri E, La Vecchia C, Luchini L, Mezzopane R. (1993) Hysterectomy, oophorectomy, and subsequent ovarian cancer. Obstet Gynecol 81:363-366
5) -Nguyen HN, Averette HE, Janicek M. (1994) Ovarian carcinoma: A review of the significance of familial risk factors and the role of prophylactic oophorectomy in cancer prevention. Cancer 74, 2:545-555
6) -Herbst AL. (1994) The epidemiology of ovarian carcinoma and the current status of tumor markers to detect disease. Am J ObstetGynecol 170, 4:1099-1107
7) -Cutler WB, (1990) Hysterectomy Before and After HarperCollins, NY.pp 40-41 and 256-257
8) -Cutler WB (1997) Pheromonal Modulation of Brain and Behavior, an invited chapter, under review in Hormonal Modulation of Brain and Behavior, American Psychiatric Press.
9) -Cutler WB and Garcia CR. (1984) The Medical Management of the Menopause and Premenopause: Their Endocrinologic Basis. Lippincott Co., Philadelphia, PA.
10) -Eggert-Kruse W, Kruse W, Rohr G, Muller S & others (1994) Hormone profile of elderly women and potential modifiers. Geburtshilfe Frauenheilkd 54, 6:321-31
11) -Carlstrom K, Brody S, Lunell NO, Lagrelius A, Mollerstrom G, Pousette A, Rannevik G, Stege R, von Schoultz B (1988) Dehydroepiandrosterone in serum: Differences related to age and sex. Maturitas 10:297-306
12) -Cumming DC, Rebar RW, Hopper BR, Yen SSC (1982) Evidence or an influence of the ovary on circulating dehydroepiandrosterone sulfate levels. J of Clinical Endocrinology & Metabolism 54, 5:1069-1071
13) -Schwartz AG, Whitcomb JM, Nyce JW, Lewbart ML, Pashko LL. (1988) Dehydroepiandrosterone and structural analogs: A new class of cancer chemopreventive agents. Advances in Cancer Research 51:391-425
14) -Mason BH, Holdaway IM, Skinner SJ, Kay RG (1994) The relationship of urinary and plasma androgens to steroid receptors and menopausal status in breast cancer patients and their influence on survival. Breast Cancer Res Treat 32, 2:203-12
15) -Barrett-Connor E, Khaw K-t, Yen S (1986) A prospective study of dehydroepiandrosterone sulfate, mortality, and cardiovascular disease. New England J of Med, 315:1519-1524
16) -Mortola JF and Yen SC (1990) The effects of oral dehydroepiandrosterone on endocrine-metabolic parameters in postmenopausal women. J Clin Endocrinol Metab 696-704.
17) -Barrett-Connor E, Goodman-Gruen D (1995) Dehydroepiandrosterone sulfate does not predict cardiovascular death in postmenopausal women. The Rancho Bernardo Study. Dept of Family & Preventive Medicine 91, 6:1757-60
18) -Nordin BEC, Robertson A, Seamark RF, Bridges A, Philcox JC, Need AG, Horowitz M, Morris HA, Deam S. (1985) The relation between calcium absorption, serum dehydroepiandrosterone, and vertebral mineral density in postmenopausal women. J of Clin Endocrinology & Metabolism 60:651-657
19) -Bodine PV, Riggs BL, Spelsberg TC (1995) Regulation of c-fos expression and TGF-beta production by gonadal and adrenal androgens in normal human osteoblastic cells. J Steroid Biochem Mol Biol 52, 2:149-58
20) -Bologna I, Sharma J, Roberts E (1987) Dehydroepiandrosterone and its sulfated derivative reduce neuronal death and enhance astrocyctic differentiation in brain cell cultures. J of Neuroscience Research 17:225-234
21) -Sunderland T, Merril CR, Harrington MG, Lawlor BA, Molchan SE, Martinez R, Murphy DL. (1989) Reduced plasma dehydroepiandrosterone concentrations in alzheimer's disease. Lancet pg 570
22) -Casson P, Faquin L, Stentz F, Straughn A, Andersen R, Abraham G, Buster J (1995) Replacement of dehydroepiandrosterone enhances T-lymphocyte insulin binding in postmenopausal women. Fertil/Steril 63:1027-1037
23) -Goldstein S, Suramanyam B, Snyder J, Beller U, Raghavendra BN, Beckman EM(1989) The postmenopausal cystic adnexal mass: The potential role of ultrasound in conservative management. Obstet Gynecol 73:8-10
24)-Weiner Z, Thaler I, Beck D, Rotten S, Deutsch M, Brandes J. (1992) Differentiating malignant from benign ovarian tumors with transvaginal colorflow imaging. Obstet Gynecol 79:159-162
25) -Brumstead JR, Blackman JA, Badger GJ, Riddick DH (1996) Hysteroscopy versus hysterectomy for the treatment of abnormal uterine bleeding: A comparison of cost. Fertility and Sterility 65:310-316
RECONOCIMIENTOS
Quisiera agradecer a Norma McCoy, Ph.D., Profesora de Sicología, San Francisco State University (Universidad Estatal de San Francisco), y a Brooke Wollenberg en el Instituto Athena por su ayuda en la preparación, investigación y la revisión de este manuscrito y conjuntamente a Elizabeth Genovese Stone, M.D. Directora Médica del Instituto Athena y a Millicent Zacher, D.O., Actuando como Director de la División de la Reproducción Endocrinóloga y de Infertilidad, Departamento de Ob/Gyn, Albert Einstein Centro Médico, Filadelfia por sus comentarios significativos sobre perspectivas médicas
Copyright (c) 1996 Athena Institute. All rights reserved.
Reproduction in whole or in part in any form or medium without express written permission of Athena Institute is prohibited
Mi investigación se ha centrado consistentemente en qué comportamiento puede adoptar una mujer para aumentar su poder, bienestar, vitalidad y placer sexual.
---Winnifred B. Cutler, Ph.D.
Una parte de las ganancias de nuestras ventas de libros y feromonas ayuda a financiar la investigación en curso de Athena.